自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明,承诺出口产品已取得我国医疗器械产品注册证书,符合进口国(地区)的质量标准要求。海关凭药品监督管理部门批准的医疗器械产品注册证书验放。
上述五种医疗物资,属于《医疗器械分类目录》管理的医疗器械,具体类别如下:
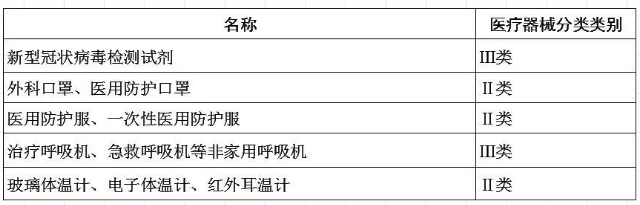
二、海关总署2020年第“53号公告”(以下简称“53号公告”)
自4月10日起,对“6307900010”等海关商品编号项下的11类医疗物资实施出口商品检验,共涉及19个HS编码。
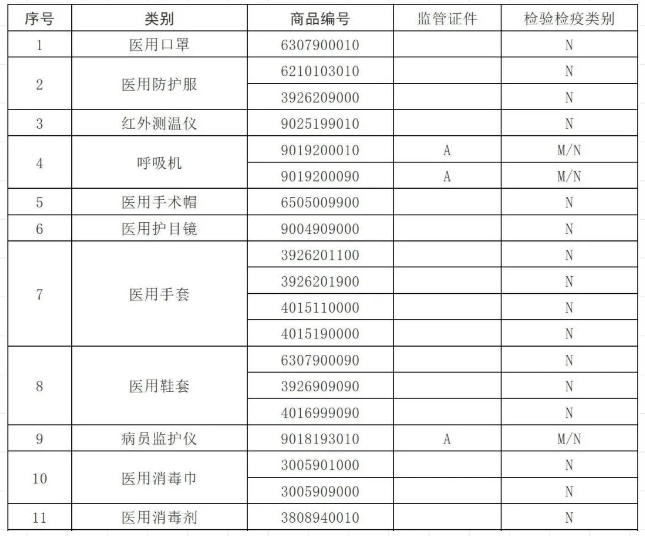
需要注意的是,“53号公告”中的11类医疗物资中,有4类与“5号公告”重合(”5号公告”中的5类医疗物资中,检测试剂此前已实施卫生检疫审批)。
法律依据
《中华人民共和国进出口商品检验法》
第五条 列入目录的进出口商品,由商检机构实施检验。
前款规定的进口商品未经检验的,不准销售、使用;前款规定的出口商品未经检验合格的,不准出口。
第十五条 本法规定必须经商检机构检验的出口商品的发货人或者其代理人,应当在商检机构规定的地点和期限内,向商检机构报检。商检机构应当在国家商检部门统一规定的期限内检验完毕,并出具检验证单。
第三十三条 违反本法规定,将必须经商检机构检验的进口商品未报经检验而擅自销售或者使用的,或者将必须经商检机构检验的出口商品未报经检验合格而擅自出口的,由商检机构没收违法所得,并处货值金额5%以上20%以下的罚款;构成犯罪的,依法追究刑事责任。
第三十五条 进口或者出口属于掺杂掺假、以假充真、以次充好的商品或者以不合格进出口商品冒充合格进出口商品的,由商检机构责令停止进口或者出口,没收违法所得,并处货值金额百分之五十以上三倍以下的罚款;构成犯罪的,依法追究刑事责任。
《中华人民共和国进出口商品检验法实施条例》
第二十四条 法定检验的出口商品的发货人应当在海关总署统一规定的地点和期限内,持合同等必要的凭证和相关批准文件向出入境检验检疫机构报检。法定检验的出口商品未经检验或者经检验不合格的,不准出口。
出口商品应当在商品的生产地检验。海关总署可以根据便利对外贸易和进出口商品检验工作的需要,指定在其他地点检验。
出口实行验证管理的商品,发货人应当向出入境检验检疫机构申请验证。出入境检验检疫机构按照海关总署的规定实施验证。
第四十四条 擅自出口未报检或者未经检验的属于法定检验的出口商品,或者擅自出口应当申请出口验证而未申请的出口商品的,由出入境检验检疫机构没收违法所得,并处商品货值金额5%以上20%以下罚款;构成犯罪的,依法追究刑事责任。
政策解读
1、海关对于“53号公告”规定的11类出口法检医疗物资,采取验证管理方式,“不实施产地检验,无需电子底账,不走e-CIQ系统”,企业可正常申报报关单。
2、“53号公告”中涉及的19个HS编码商品中,医用的才需要实施出口商品检验。对于是否属于医用物资,海关监管时根据商品本身特征而非申报用途进行判定。
判定标准详情请参见:我国和国外部分国家(地区)防疫医疗物资标准和主要项目(第一版)
链接:
http://sjs.customs.gov.cn/sjs/zcfg56/2963129/index.html?from=groupmessage
监管措施
一、加强单证审核
“53号公告”是海关针对医疗物资的监管措施,不涉及非医疗物资,因此,申报系统中未对“53号公告”中的19个HS编码商品设置出口商品检验监管条件。海关采取电子审核加人工审单的方法处理“53号公告”涉及的申报单证。
(1)对“5号公告”所列(含公告后续调整所列)的5类医疗物资,企业向海关报关时,须提供书面或电子质量安全承诺声明和我国医疗器械产品注册证书。新冠病毒检测试剂还须提供药监部门出具的出口销售证明。
(2)对“53号公告”所列“5号公告”以外的7类医疗物资,企业向海关报关时,应当提供医疗器械产品注册(Ⅲ类/Ⅱ类医疗器械)/备案(Ⅰ类医疗器械)证明和质量安全承诺声明。对无相关证明和承诺声明的,海关将实施严密监管。
(3)对新冠病毒检测试剂,发货人还应当申请卫生检疫审批,凭《入/出境特殊物品卫生检疫审批单》通过单一窗口报检,经海关检验合格后,获得电子底账,报关时填写电子底账帐号。
(4)对出口法检医疗物资,建议企业在报关单商品名称栏填报用途,并注明是否医用,检测试剂注明是否为新型冠状病毒检测用。
海关将对医疗器械产品注册证书和企业质量安全承诺声明进行严格审核,重点审核是否存在缺失、冒用、伪造医疗器械产品注册证书的情形,核对证书编号是否与国家药监局网站是否一致。
二、严格现场查验
海关现场查验部门根据布控指令实施查验,对发现异常的实施彻底查验,必要时抽样送有资质的实验室检测。
出口法检医疗物资应当符合进口国(地区)的要求,对进口国(地区)无质量安全标准要求的,应当符合我国质量安全标准。
详情请参见:部分国家(地区)防疫物资技术法规和标准要求(第三版)
链接:
http://sjs.customs.gov.cn/sjs/zcfg56/2951967/index.html
三、严厉打击违法违规行为
海关对存在质量安全问题的出口防疫物资依法依规实施快速处置;对发现企业有出口防疫物资伪瞒报、夹藏夹带、掺杂掺假、以假充真、以次充好或者以不合格冒充合格等违法行为的,依法依规进行严厉查处;涉嫌犯罪的,移送地方公安机关追究刑事责任。
企业的违法情况将纳入企业信用记录,并将作为海关风险管理和信用管理的重要依据;海关将相关信息共享至全国信用信息共享平台,由有关部门对海关失信企业实施联合惩戒。
问题答疑
Q:疫情初期,由于国内口罩等医疗防疫物资产量低无法满足防疫需求,一些企业响应国家的号召,紧急购买设备生产口罩等疫情防疫物资,当时省级药监部门临时批准了医疗器械应急注册证书,相关企业陆续投产并生产出大量的口罩等医疗防疫物资,为成功抗疫作出了贡献。如疫情期间获医疗器械应急注册证书的企业未在国家药监局网站公布的企业名录内,能正常出口吗?
A:海关进行单证审核时依据国家药监局公布的企业名录进行验证。据了解,部分省份通过快速审批程序,已将前期获应急/临时注册证书的企业维护进国家药监局网站公布的企业名录,相关企业可以出口。相关详情企业可咨询当地药品监督管理部门。
Q:企业和个人如何根据商品本身特征判定医用/非医用?
A:不同用途的防疫产品其技术要求不同、适用范围也不同。一是可以利用外观与包装信息进行区分。正规途径销售的防疫产品的最小单元包装上应该有商品名称、执行的标准和防护等级等信息,这些商家明示的信息可以作为一个分辨点。以口罩为例,如商品名称中带有“医用”或英文“surgical”“Medical”等字样的,一般可判定为医用口罩;二是可以根据适用标准进行区分。医用/非医用产品适用不同的标准和认证要求,企业和个人可根据产品外包装或生产者提供的检测报告或证书上的产品适用标准和认证信息来进行判断。
Q:医用消毒剂如属于危险化学品的如何实施出口商品检验?
A:如属于危险化学品的应按原有要求实施产地检验(如属于危险货物的还需实施危险货物包装检验鉴定),同时按照“53号公告”要求实施口岸检验。
信息来源:海关发布


地址:汕头市龙湖区珠城路28号国瑞会展中心1幢1605室
电话:(+86754)87223298
传真:(+86754)87223211 电子邮箱:stccie@126.com 粤ICP备19138642号
技术支持:Micronet微网 管理员入口

手机版

APP版
版权所有:汕头市进出口商会 粤公网安备 44050702000262号


